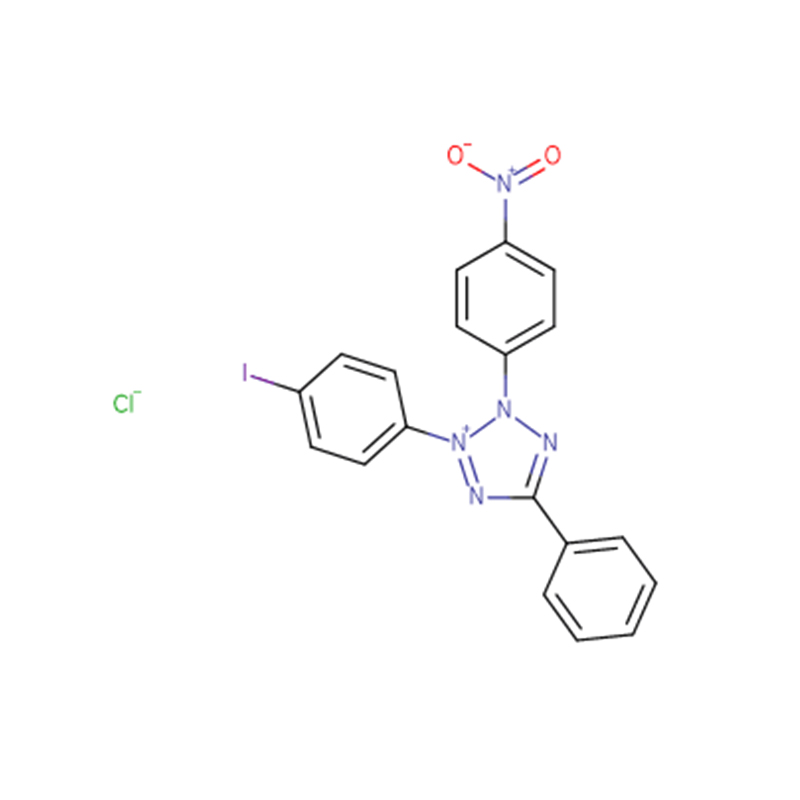
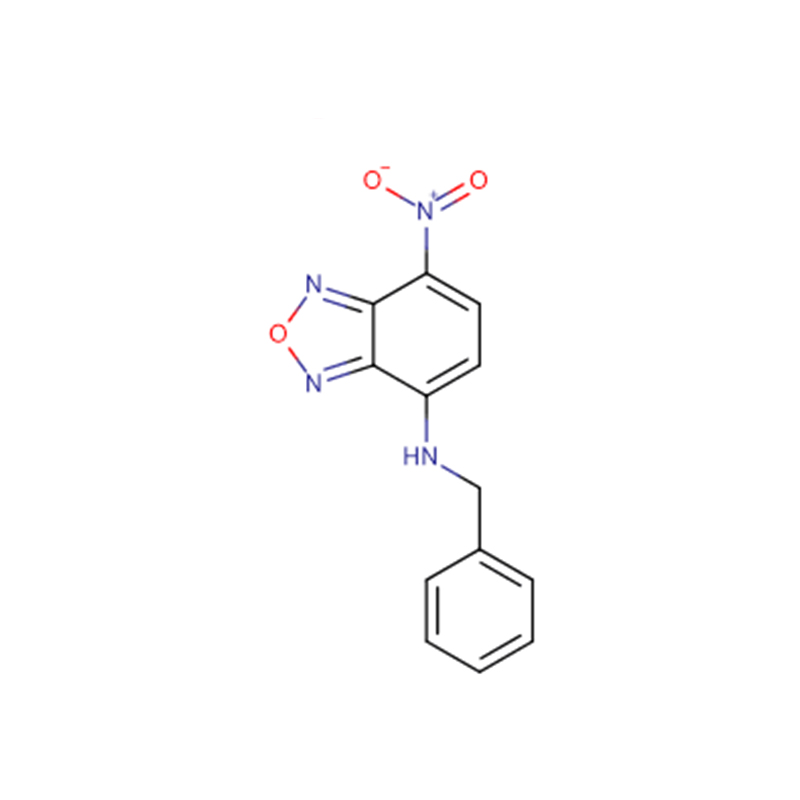
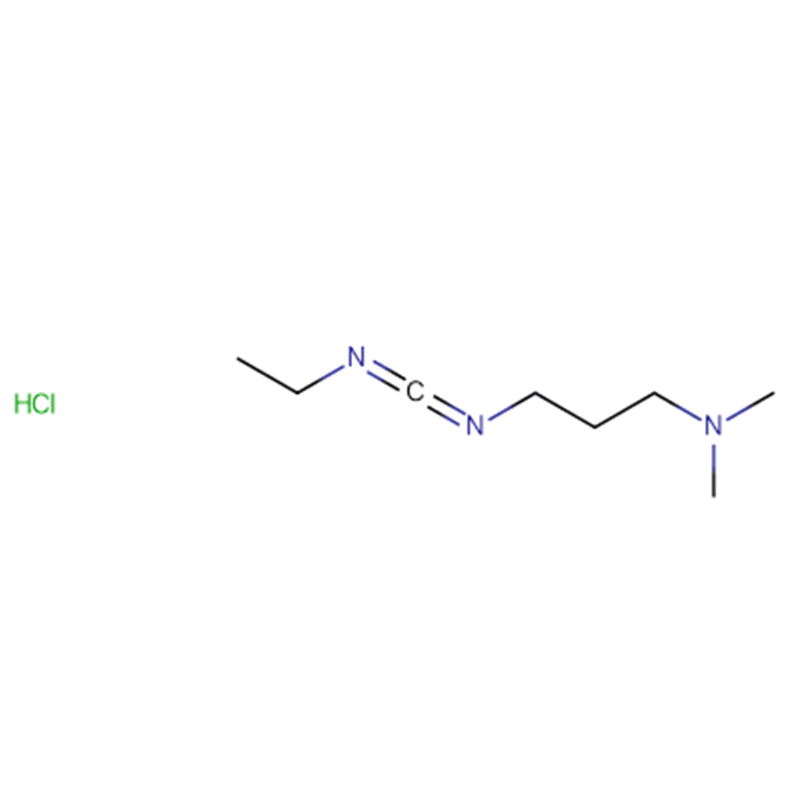
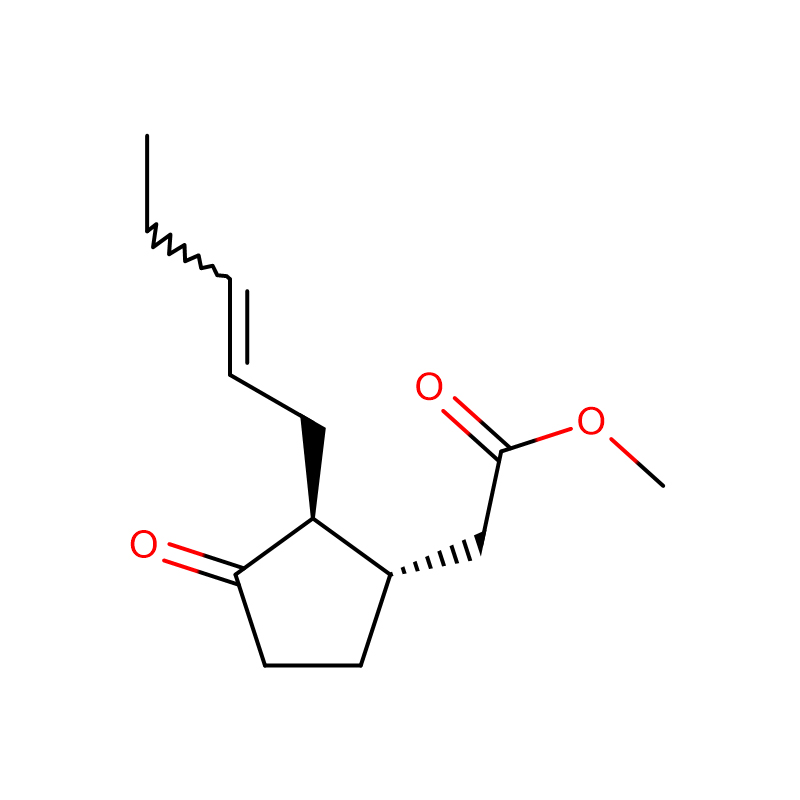
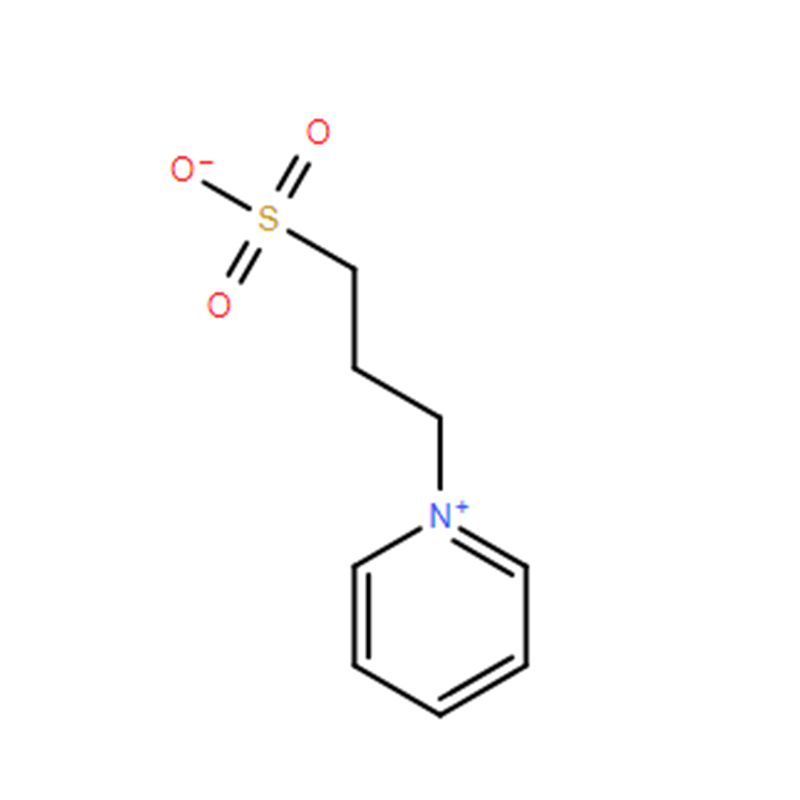
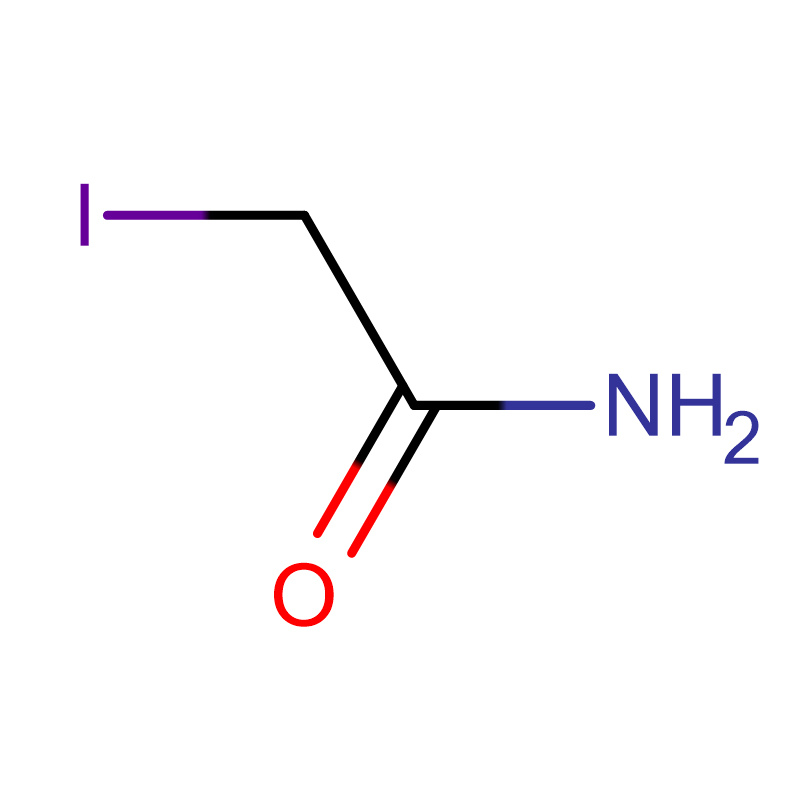
Iodonitrotetrazolium chloride Cas: 146-68-9 98% Lysegult til orange pulver
| Katalognummer | XD90217 |
| produktnavn | Iodonitrotetrazoliumchlorid |
| CAS | 146-68-9 |
| Molekylær formel | C19H13ClIN5O2 |
| Molekylær vægt | 505,70 |
| Opbevaringsdetaljer | 2 til 8 °C |
| Harmoniseret tarifkode | 32129000 |
Produkt specifikation
| Identifikation | H-NMR |
| Opløselighed | Klar løsning |
| Udseende | Lysegult til orange pulver |
| Assay HPLC | >98 % |
En gensidig translokation af ABL1-genet til BCR-genet resulterer i ekspressionen af det onkogene BCR-ABL1-fusionsprotein, som karakteriserer human kronisk myeloid leukæmi (CML), en myeloproliferativ lidelse, der betragtes som uvægerligt dødelig indtil introduktionen af imatinib-familien af tyrosinkinase hæmmere (TKI).Ikke desto mindre er ufølsomhed af CML-stamceller over for TKI-behandling og iboende eller erhvervet resistens stadig hyppige årsager til sygdomspersistens og blastisk faseprogression oplevet hos patienter efter indledende vellykkede terapier.Her undersøgte vi en mulig rolle for MAPK15/ERK8-kinasen i BCR-ABL1-afhængig autofagi, en nøgleproces for onkogen-induceret leukomogenese.I denne sammenhæng viste vi MAPK15's evne til fysisk at rekruttere onkogenet til autofagiske vesikler, hvilket bekræfter vores hypotese om en biologisk relevant rolle for denne MAP-kinase i signaltransduktion af dette onkogen.Ved at modellere BCR-ABL1-signalering i HeLa-celler og drage fordel af en fysiologisk relevant model for human CML, dvs. K562-celler, viste vi, at BCR-ABL1-induceret autofagi medieres af MAPK15 gennem dets evne til at interagere med LC3-familien proteiner på en LIR-afhængig måde.Interessant nok var vi også i stand til at interferere med BCR-ABL1-induceret autofagi ved en farmakologisk tilgang rettet mod at hæmme MAPK15, hvilket åbner muligheden for at virke på denne kinase for at påvirke autofagi og sygdomme afhængigt af denne cellulære funktion.For at understøtte gennemførligheden af denne tilgang demonstrerede vi faktisk, at udtømning af endogen MAPK15-ekspression inhiberede BCR-ABL1-afhængig celleproliferation, in vitro og tumordannelse, in vivo, hvilket giver en ny "medicinsk" forbindelse mellem BCR-ABL1 og human CML.