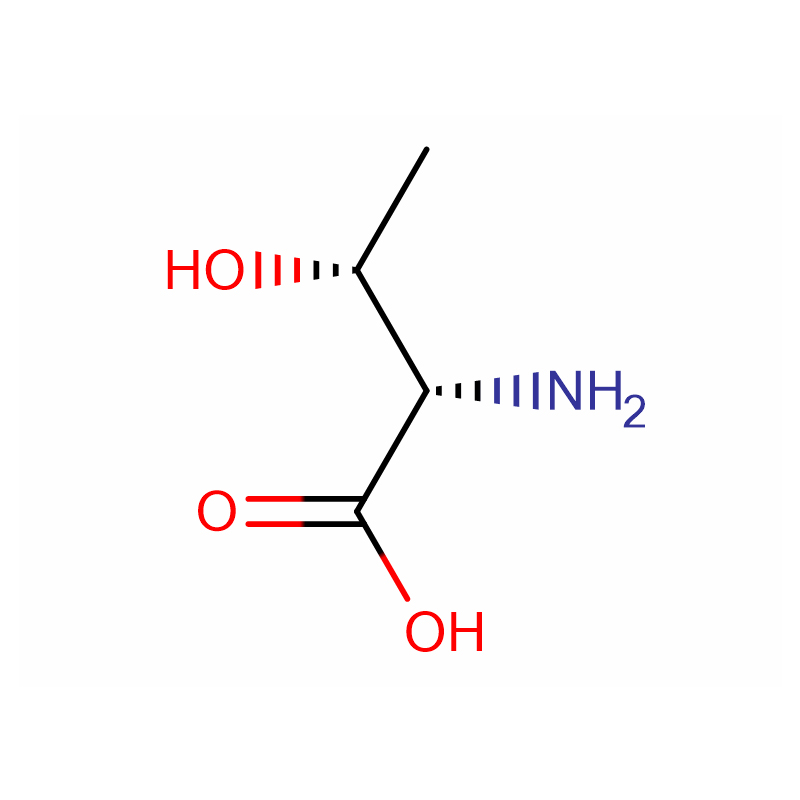
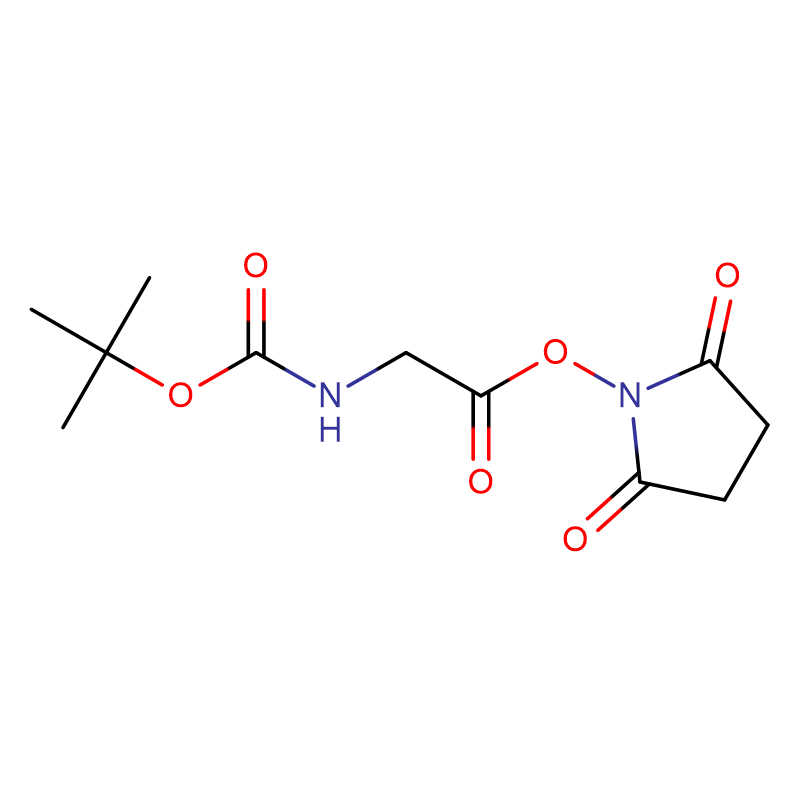
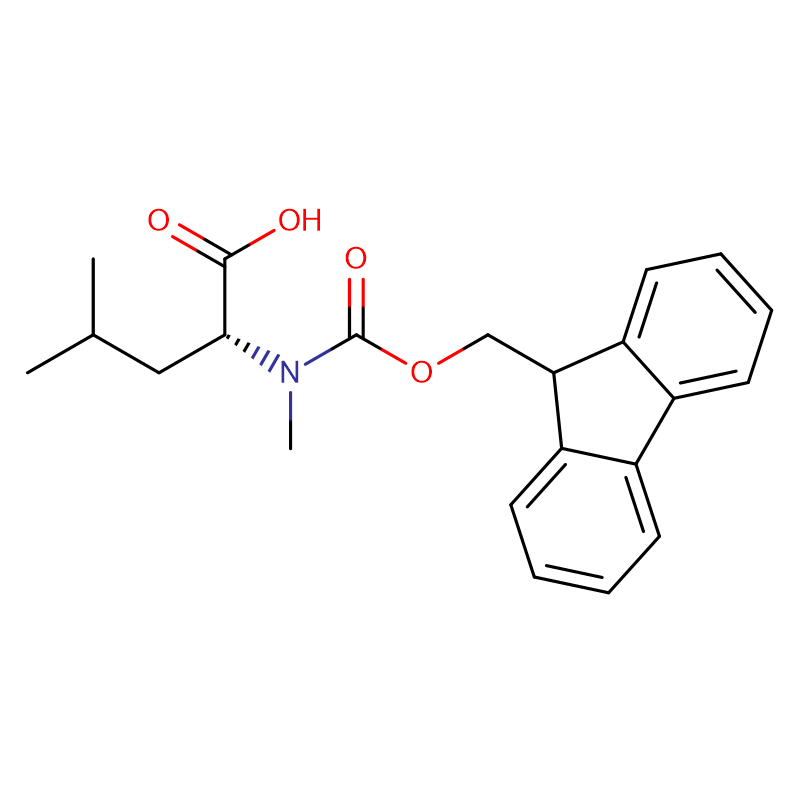
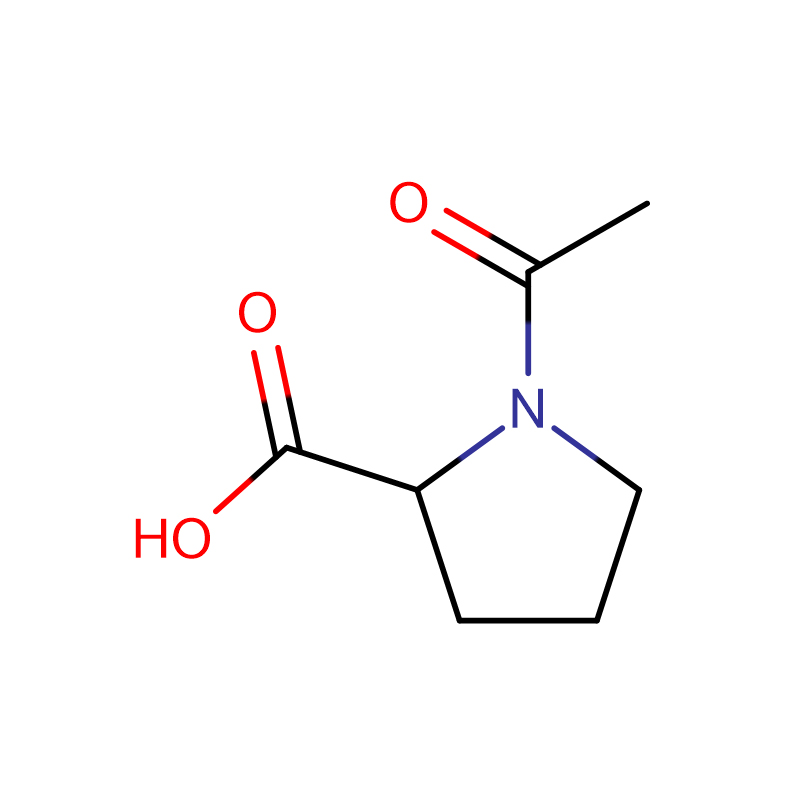
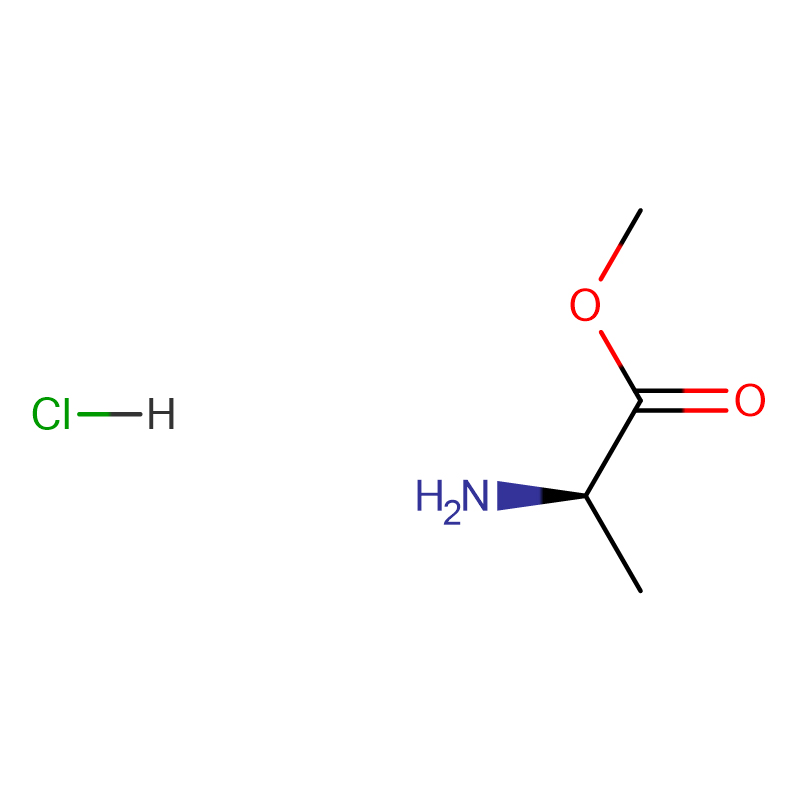
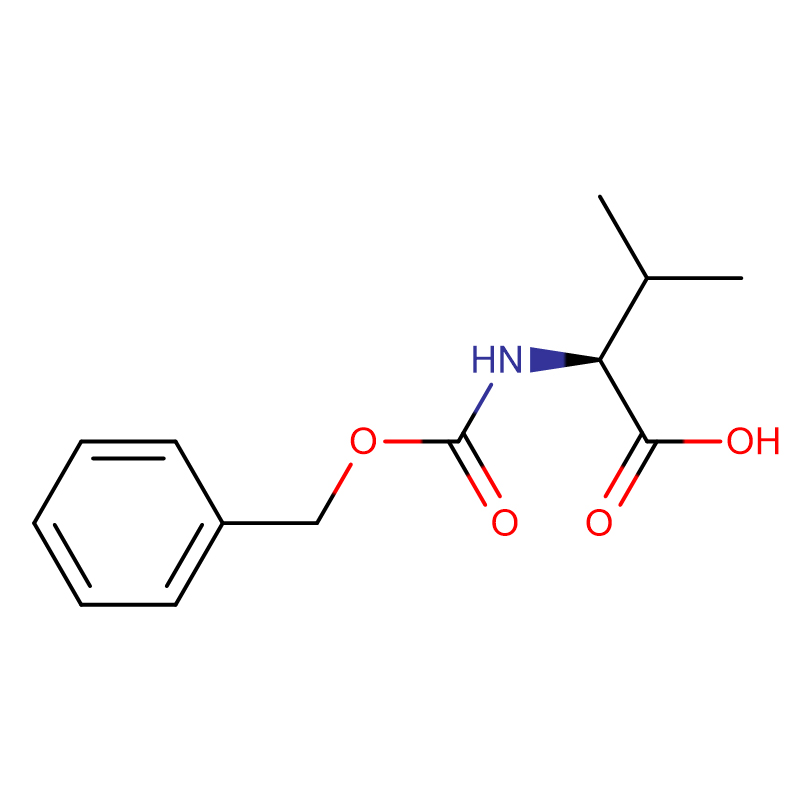
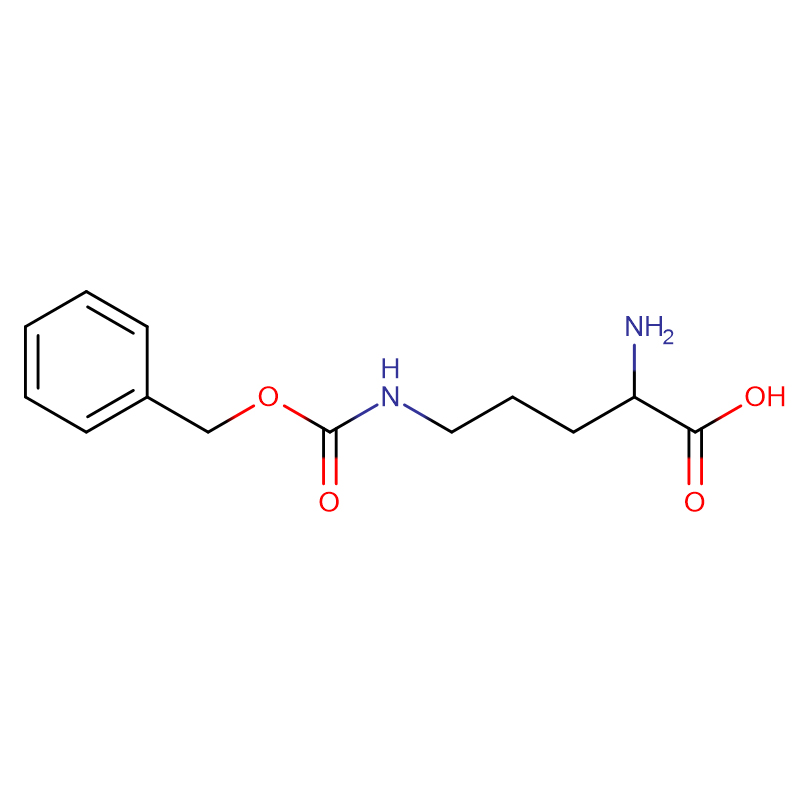
(2S,3R)-2-Amino-3-hydroxybutansyre Cas: 72-19-5 99% Hvidt krystallinsk pulver
| Katalognummer | XD90285 |
| produktnavn | (2S,3R)-2-amino-3-hydroxybutansyre |
| CAS | 72-19-5 |
| Molekylær formel | C4H9NO3 |
| Molekylær vægt | 119.11916 |
| Opbevaringsdetaljer | Ambient |
| Harmoniseret tarifkode | 29225000 |
Produkt specifikation
| Assay | 99 - 101 % |
| Udseende | Hvidt krystallinsk pulver |
| Specifik rotation | -27,5 til -29,0 |
| Tungmetaller | 10 ppm Maks. |
| AS | 10 ppm maks |
| pH | 5,2 - 6,5 |
| SO4 | <0,020 % |
| Fe | 10 ppm maks |
| Tab ved tørring | <0,20 % |
| Restprodukt ved antænding | <0,10 % |
| Transmission | NLT 98 % |
| Cl | <0,02 % |
| Ammoniumsalt | <0,02 % |
Serin/threoninproteinphosphataser er blevet beskrevet i mange patogene bakterier som essentielle enzymer involveret i phosphoryleringsafhængige signaltransduktionsveje og ofte forbundet med disse organismers virulens.En inspektion af Mycoplasma synoviae-genomet afslørede tilstedeværelsen af et gen (prpC), der koder for en formodet proteinphosphatase fra proteinphosphatase 2C (PP2C) underfamilien.Her rapporterer vi en komplet biokemisk karakterisering af M. synoviae phosphatase (PrpC) og den særlige rolle af metalioner i struktur-funktion forholdet af dette enzym.PrpC-aminosyresekvensanalyse afslørede, at alle resterne involveret i det dinukleære metalcenter og de formodede tredje metalion-koordinerende rester, konserveret i PP2C-phosphataser, er til stede i PrpC.PrpC er et monomert protein i stand til at dephosphorylere phospho-substrater med Mn(2+)-ioners afhængighed.Termisk stabilitetsanalyse viste enzymstabiliteten ved milde temperaturer og påvirkningen af Mn(2+)-ioner i denne egenskab.Massespektrometrianalyse antydede, at tre metalioner binder til PrpC, hvoraf to med en tilsyneladende højaffinitetskonstant.Mutationsanalyse af de formodede tredje metal-koordinerende rester, Asp122 og Arg164, afslørede, at disse varianter udviste en svagere binding af manganioner, og at begge mutationer påvirkede PrpC-phosphataseaktivitet.Ifølge disse resultater er PrpC et metalafhængigt proteinphosphatase-medlem med en forbedret stabilitet i holo-formen og med Asp122, muligvis impliceret i det tredje metalbindingssted, essentielt for katalytisk aktivitet.